Dosage de complémentation de fragments protéiques
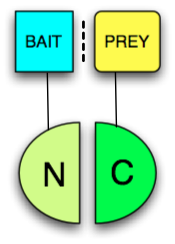
le dosage de complémentation de fragments protéiques (PCA pour Protein-fragment Complementation Assay), est une technique de biologie moléculaire consistant à quantifier des interactions protéine-protéine en couplant chacune des deux protéines d'intérêt avec des fragments d'une troisième protéine et en testant la restauration de son activité. Les protéines d'intérêt (« appât » et « proie ») sont chacune liées de manière covalente à des fragments d'une « protéine rapporteuse » ((par exemple, la DHFR ou la luciférase, entre autres). Si les protéines appât et proie interagissement, elles permettent aux 2 fragments du rapporteur de se rapprocher. Celui-ci devient fonctionnel et on peut en mesurer l'activité.
Cette technique présente l'avantage de présenter moins de faux positifs que le double hybride. On peut la perfectionner en rajoutant des séquences d'intégrine entre protéine et sous-unité catalytique. L'intégrine, qui est une ligase, établit une liaison covalente entre les 2 protéines et reformer la luciférase.
Ce principe s'applique à de nombreuses protéines rapporteuses et constitue également la base du système double hybride de la levure, un test PCA archétypal.
Cependant, toutes les protéines ne peuvent être utilisées comme rapporteuse, en effet, il faut qu'elles possèdent des domaines bien distincts qui soient solubles lorsqu'ils sont séparés l'un de l'autre.
Rapporteurs
[modifier | modifier le code]Toute protéine pouvant être scindée en deux fragments et reconstituée de manière non covalente pour former une protéine fonctionnelle peut être utilisée en PC). Toutefois, les deux fragments doivent présenter une faible affinité l'un pour l'autre de façon à n'être rapprochés que par les protéines interagissantes auxquelles ils sont liés (« appât » et « proie »), car la protéine appât permet d'identifier la protéine proie, voir figure). La protéine produisant un signal détectable est appelée « rapporteur ». Généralement, on utilise comme rapporteurs des enzymes conférant une résistance à la privation de nutriments ou aux antibiotiques, telles que la dihydrofolate-réductase ou la bêta-lactamase, ou des protéines émettant des signaux colorimétriques ou fluorescents. Lorsque des protéines fluorescentes sont reconstituées, le test PCA est appelé test de complémentation de fluorescence bimoléculaire.
Les protéines suivantes ont été utilisées dans les PCA à protéines scindées :
- Bêta-lactamase[1],[2] ;
- Dihydrofolate-réductase (DHFR)[3] ;
- Kinase d’adhésion focale (FAK)[4] ;
- Gal4, un facteur de transcription de levure (comme dans le système classique à double hybride de levure) ;
- GFP (GFP scindée), par exemple EGFP (protéine fluorescente verte améliorée)[5],[6],[7] ;
- Peroxydase de raifort[8] ;
- Protéine fluorescente infrarouge IFP1.4, un domaine de liaison au chromophore (CBD) modifié d’un bactériophytochrome de Deinococcus radiodurans[9] ;
- LacZ (bêta-galactosidase)[10] ;
- Luciférase[11],[12], dont ReBiL (luciférase bimoléculaire améliorée par recombinase)[13] et la luciférase de Gaussia princeps (en)[14] ; parmi les produits commerciaux utilisant la luciférase, on trouve NanoLuc et NanoBIT[15] ; une modification a également été développée pour les interactions associées aux gouttelettes lipidiques[16] ;
- FAST (splitFAST)[17] ;
- TEV (protéase du virus de la mosaïque du tabac)[18] ;
- Ubiquitine[19].
Application à l'échelle du génome
[modifier | modifier le code]Les méthodes mentionnées ci-dessus ont été appliquées à des génomes entiers, par exemple celui de la levure[3] ou de la bactérie de la syphilis[20].
Références
[modifier | modifier le code]- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Protein-fragment complementation assay » (voir la liste des auteurs).
- ↑ Park JH, Back JH, Hahm SH, Shim HY, Park MJ, Ko SI, Han YS, « Bacterial beta-lactamase fragmentation complementation strategy can be used as a method for identifying interacting protein pairs », Journal of Microbiology and Biotechnology, vol. 17, no 10, , p. 1607–15 (PMID 18156775)
- ↑ Remy I, Ghaddar G, Michnick SW, « Using the beta-lactamase protein-fragment complementation assay to probe dynamic protein-protein interactions », Nature Protocols, vol. 2, no 9, , p. 2302–6 (PMID 17853887, DOI 10.1038/nprot.2007.356, S2CID 7607566)
- Tarassov K, Messier V, Landry CR, Radinovic S, Serna Molina MM, Shames I, Malitskaya Y, Vogel J, Bussey H, Michnick SW, « An in vivo map of the yeast protein interactome », Science, vol. 320, no 5882, , p. 1465–70 (PMID 18467557, DOI 10.1126/science.1153878, Bibcode 2008Sci...320.1465T, S2CID 1732896, lire en ligne)
- ↑ Yidan Ma, Teruyuki Nagamune et Masahiro Kawahara, « Split focal adhesion kinase for probing protein–protein interactions », Biochemical Engineering Journal, vol. 90, , p. 272–278 (DOI 10.1016/j.bej.2014.06.022, Bibcode 2014BioEJ..90..272M)
- ↑ Barnard E, Timson DJ, Molecular and Cell Biology Methods for Fungi, vol. 638, coll. « Methods in Molecular Biology », , 303–17 p. (ISBN 978-1-60761-610-8, PMID 20238279, DOI 10.1007/978-1-60761-611-5_23), « Split-EGFP Screens for the Detection and Localisation of Protein–Protein Interactions in Living Yeast Cells »
- ↑ Blakeley BD, Chapman AM, McNaughton BR, « Split-superpositive GFP reassembly is a fast, efficient, and robust method for detecting protein-protein interactions in vivo », Molecular BioSystems, vol. 8, no 8, , p. 2036–40 (PMID 22692102, DOI 10.1039/c2mb25130b)
- ↑ Cabantous S, Nguyen HB, Pedelacq JD, Koraïchi F, Chaudhary A, Ganguly K, Lockard MA, Favre G, Terwilliger TC, Waldo GS, « A new protein-protein interaction sensor based on tripartite split-GFP association », Scientific Reports, vol. 3, (PMID 24092409, PMCID 3790201, DOI 10.1038/srep02854, Bibcode 2013NatSR...3.2854C)
- ↑ Martell JD, Yamagata M, Deerinck TJ, Phan S, Kwa CG, Ellisman MH, Sanes JR, Ting AY, « A split horseradish peroxidase for the detection of intercellular protein-protein interactions and sensitive visualization of synapses », Nature Biotechnology, vol. 34, no 7, , p. 774–80 (PMID 27240195, PMCID 4942342, DOI 10.1038/nbt.3563, lire en ligne)
- ↑ Tchekanda E, Sivanesan D, Michnick SW, « An infrared reporter to detect spatiotemporal dynamics of protein-protein interactions », Nature Methods, vol. 11, no 6, , p. 641–4 (PMID 24747815, DOI 10.1038/nmeth.2934, S2CID 1958433)
- ↑ Rossi F, Charlton CA, Blau HM, « Monitoring protein-protein interactions in intact eukaryotic cells by beta-galactosidase complementation », Proceedings of the National Academy of Sciences of the United States of America, vol. 94, no 16, , p. 8405–10 (PMID 9237989, PMCID 22934, DOI 10.1073/pnas.94.16.8405
 , Bibcode 1997PNAS...94.8405R)
, Bibcode 1997PNAS...94.8405R)
- ↑ Cassonnet P, Rolloy C, Neveu G, Vidalain PO, Chantier T, Pellet J, Jones L, Muller M, Demeret C, Gaud G, Vuillier F, Lotteau V, Tangy F, Favre M, Jacob Y, « Benchmarking a luciferase complementation assay for detecting protein complexes », Nature Methods, vol. 8, no 12, , p. 990–2 (PMID 22127214, DOI 10.1038/nmeth.1773, S2CID 9377872)
- ↑ Fujikawa, Y. et al. (2014) Split luciferase complementation assay to detect regulated protein-protein interactions in rice protoplasts in a large-scale format. Rice 7:11
- ↑ Li YC, Rodewald LW, Hoppmann C, Wong ET, Lebreton S, Safar P, Patek M, Wang L, Wertman KF, Wahl GM, « A versatile platform to analyze low-affinity and transient protein-protein interactions in living cells in real time », Cell Reports, vol. 9, no 5, , p. 1946–58 (PMID 25464845, PMCID 4269221, DOI 10.1016/j.celrep.2014.10.058)
- ↑ Neveu G, Cassonnet P, Vidalain PO, Rolloy C, Mendoza J, Jones L, Tangy F, Muller M, Demeret C, Tafforeau L, Lotteau V, Rabourdin-Combe C, Travé G, Dricot A, Hill DE, Vidal M, Favre M, Jacob Y, « Comparative analysis of virus-host interactomes with a mammalian high-throughput protein complementation assay based on Gaussia princeps luciferase », Methods, vol. 58, no 4, , p. 349–59 (PMID 22898364, PMCID 3546263, DOI 10.1016/j.ymeth.2012.07.029)
- ↑ Brock Binkowski, Christopher Eggers, Braeden Butler, Marie Schwinn, Michael Slater, Thomas Machleidt, Mei Cong, Keith Wood et Frank Fan, « Monitoring intracellular protein interactions using NanoLuc® Binary Technology (NanoBiTTM) », Promega,
- ↑ Kolkhof P, Werthebach M, van de Venn A, Poschmann G, Chen L, Welte M, Stühler K, Beller M, « A Luciferase-fragment Complementation Assay to Detect Lipid Droplet-associated Protein-Protein Interactions », Molecular & Cellular Proteomics, vol. 16, no 3, , p. 329–345 (PMID 27956707, PMCID 5340998, DOI 10.1074/mcp.M116.061499
 )
)
- ↑ (en) Alexandra M. Bendel, Andre J. Faure, Dominique Klein, Kenji Shimada, Romane Lyautey, Nicole Schiffelholz, Georg Kempf, Simone Cavadini, Ben Lehner et Guillaume Diss, « The genetic architecture of protein interaction affinity and specificity », Nature Communications, vol. 15, no 1, , p. 8868 (ISSN 2041-1723, PMID 39402041, PMCID 11479274, DOI 10.1038/s41467-024-53195-4, Bibcode 2024NatCo..15.8868B)
- ↑ Wehr MC, Laage R, Bolz U, Fischer TM, Grünewald S, Scheek S, Bach A, Nave KA, Rossner MJ, « Monitoring regulated protein-protein interactions using split TEV », Nature Methods, vol. 3, no 12, , p. 985–93 (PMID 17072307, DOI 10.1038/nmeth967, S2CID 37120401)
- ↑ Dünkler A, Müller J, Johnsson N, Gene Regulatory Networks, vol. 786, coll. « Methods in Molecular Biology », , 115–30 p. (ISBN 978-1-61779-291-5, PMID 21938623, DOI 10.1007/978-1-61779-292-2_7), « Detecting Protein–Protein Interactions with the Split-Ubiquitin Sensor »
- ↑ Björn Titz, Seesandra V. Rajagopala, Johannes Goll, Roman Häuser, Matthew T. McKevitt, Timothy Palzkill et Peter Uetz, « The binary protein interactome of Treponema pallidum--the syphilis spirochete », PLOS ONE, vol. 3, no 5, (ISSN 1932-6203, PMID 18509523, PMCID 2386257, DOI 10.1371/journal.pone.0002292
 , Bibcode 2008PLoSO...3.2292T)
, Bibcode 2008PLoSO...3.2292T)
