Canis
Loups (Lato sensu), Chacals (Lato sensu)
Un loup (C. lupus), un chien (C. familiaris) ;
Un loup rouge (C. rufus), un Loup de l'Est (C. lycaon) ;
Un coyote (C. latrans), un chacal (C. aureus) ;
- Alopsis Rafinesque, 1815[1]
- Thos Oken, 1816[2]
- Lupus S.D.W., 1836[3]
- Vulpicanis de Blainville, 1837[4]
- Lyciscus C.H. Smith, 1839[5]
- Oxygous Hodgson, 1841[6]
- Lupulus Gervais, 1855[7]
- Simenia J.E. Gray, 1868[8]
- Dieba J.E. Gray, 1869[9]
- Lycorus Bourguignat, 1875[10]
- Synagodus Cope, 1879[11]
- Macrocyon Ameghino, 1881[12]
- Pachycyon J.A. Allen, 1885[13]
- Mamcanisus Herrera, 1899[14]
- Alopedon Hilzheimer, 1906[15]
- Thos Heller, 1914[16]
- Oreocyon Krumbiegel, 1949[17]
- Cubacyon Arredondo de la Mata & Varona, 1974[18]
- Indocyon Arredondo de la Mata, 1981[19]
Canis est un genre de mammifères carnivores de la famille des Canidés. Ce groupe nominal comprend le chien et ses nombreuses variations domestiques ou férales, le loup et ses nombreuses sous-espèces, ainsi que d’autres espèces de canidés, toutes réparties à travers tout les continent du monde à l’exception de l’antarctique, tantôt désignées sous le terme de « loup » ou celui de « chacal » au sens large ; le chacal commun en Eurasie, le coyote (ou chacal aboyeur) en Amérique du Nord, ainsi que le loup d’Abyssinie et le loup doré en Afrique.
Les espèces de ce genre se distinguent par leur taille allant de moyenne à grande, leur crâne et leur dentition massifs et bien développés, leurs longues pattes ainsi que leurs oreilles et leur queue relativement courte[20]. Ils sont également caractérisés par leur pupilles rondes.
La classification ou le statut de certaines populations est encore incertain car les Canidés forment une famille biologique qui n'a évolué que récemment et des croisements fertiles ont eu lieu et se perpétuent encore entre certaines espèces du genre Canis, compliquant d'autant plus les recherches faites sur les différents groupes dans ce taxon, dont l'histoire est également difficile à retracer tant les vestiges sont délicats à différencier[21],[22]. Par exemple, certaines espèces encore récemment incluses dans le genre Canis sont désormais considérées former un genre distinct, Lupulella[23],[24].
Dénominations
[modifier | modifier le code]Dénomination latines
[modifier | modifier le code]Le nom du genre, Canis, provient directement du latin canis signifiant « chien », et le terme Lupus, loup.
Les espèces de plus petite taille comme le chacal doré (Canis aureus) ont pendant un temps, entre autres, été désignés sous divers noms de genres spécifiques : d’abord Thos et Thous, termes issus du grec ancien θώς pour un carnivore sauvage[2], le Chacal. Le nom « petit loup », donne Lyciscus du grec ancien λύκος (lýkos)[5], ou de latin Lupulus, qui donnera le nom de genre Lupulella. L’on retrouve aussi des noms faisant référence à la ressemblance du chacal avec le renard : Alopsis : du grec αλωπός (alōpos), « semblable à un renard »[1], ainsi que Vulpicanis : mélange de Vulpes (renard) et Canis (chien)[4]. Oxygous : du grec όξύγοος (oksygoos), « cri perçant »[6] ou Dieba : d'après le nom local nord-africain Dhibb, du l’espèce Canis lupaster[9], font référence au hurlement du de l’animal.
D’autres noms proviennet de zones géographiques comme Simenia : d'après les Monts Simien en Éthiopie[8] ou encore Cubacyon : construit sur le nom de l'île de Cuba et du grec κυων (kuōn), « chien »[18].
Les noms Synagodus (dents serrées) et Dysodus (mauvaises dents)[11] ont été utilisés pour désigner des espèces fossiles.
Noms vernaculaire : Chien, loup ou chacal ?
[modifier | modifier le code]Les noms vernaculaires « Chien », « Loup » et « Chacal » étant extrêmement récurrent en zoologie, présent dans les noms vulgaires d’un certain nombre d’espèces de canidés, de nombreuses confusions se sont installées au fil du temps. Généralement, on qualifie au sens large de « Loup » des canidés lupoïdes de grande taille, et de « Chacal » des canidés lupoïdes plus petits.
Mais formellement, au sens strict, il n’existe qu’une seule espèce de chiens : Canis familiaris, qu’une seule espèce de loup : Canis lupus, ainsi qu’une seule espèce de Chacal : Canis aureus.
De même, ce que l’on appelle aujourd’hui « Coyote » (Canis latrans), était autrefois désigné sous les termes de « Loup des prairies » ou « Chacal américain ». Chez Canis simensis, que l’on appelle le plus souvent « Loup d’Abyssinie », porte également le nom de « Chacal des simiens » ainsi que le nom spécifique de « Cabéru ». Chez Canis lupaster, appelé et francisé sous le nom de « Dhibb » en Afrique du Nord, la petite sous-espèce sénégalaise Canis lupaster anthus, est appelée « Chacal du Sénégal », là où la sous-espèce nord africaine plus grande Canis lupaster lupaster est appelée « loup d’Égypte ». Des noms vernaculaire spécifiques pourraient être utilisés pour chaque espèces, mais ce serait sans compter plusieurs problèmes :
- certaines espèces de canidés ne disposent pas de leur propre dénomination vernaculaire et sont contraintes d’être désignées sous une appellation vulgaire. C’est notamment le cas d’espèces autrefois considérées comme des sous-espèces, comme le Loup rouge (Canis rufus) et le loup de l’Est (Canis lycaon), pas assez différents sémantiquement et symboliquement du loup pour être culturellement identifiables en tant qu’entités spécifique dans l’imaginaire collectif ;
- de nombreux noms utilisés de canidés proviennent de traductions de l’anglais vers le français : pour Canis simensis et Canis lupaster, si les appellations « Cabéru » et « Dhibb » existent en français, elles n’existent pas en anglais, ce qui in fine amoindrit leur utilisation en français au profit de traductions de noms anglais ou de noms sémantiquement comparables.
Taxinomie et systématique
[modifier | modifier le code]Histoire
[modifier | modifier le code]Le genre Canis a été conceptualisé pour la première fois dans la taxonomie moderne dès la première édition du Systema Naturæ de Carl von Linné. Il s’agit du genre nominal de la famille des Canidés. Dans la première édition, le genre est représenté par des espèces appelées familiaris, lupus, lagopus et vulpes. Les espèces issues de la dixième édition du Systema Naturæ sont[25] :
Par la suite, de nombreuses espèces de canidés passeront par ce nom de genre dans le protonyme : c’est le cas des canidés lupoïdes, comme les genres Lycaon (Canis pictus), Cuon (Canis alpinus), ainsi que le Lupullella (comme Canis adustus) jusqu’en 2019 ; mais c’est également le cas des renards (genre Vulpes) comme le Fennec (autrefois Canis cetza), ainsi que d’autres canidés vulpoïdes, les genre Otocyon (autrefois Canis megalotis : Chien oreillard), ou encore Nyctereutes (autrefois Canis viverrinus : Chien viverrin), des retards taxonomiques qui peuvent entraîner un certain nombre de confusions.
Classification
[modifier | modifier le code]Toutes les espèces au sein de Canis sont étroitement liées sur le plan phylogénétique, possèdent 78 chromosomes et peuvent potentiellement s'hybrider entre elles[26]. En 1926, la Commission internationale de nomenclature zoologique (ICZN), dans son Opinion 91, a inclus le genre Canis dans ses « Listes et index officiels des noms en zoologie »[27]. En 1955, la Direction 22 de l'ICZN a ajouté Canis familiaris comme espèce type du genre Canis à la liste officielle[28].
« Canis est primitif par rapport à Cuon, Lycaon et Xenocyon de par ses canines relativement plus grandes et l'absence d'adaptations dentaires pour l'hypercarnivorie, telles que des métaconides et entoconides m1–m2 petits ou absents ; un hypocône M1–M2 petit ; un cingulum lingual M1–M2 faible ; des M2 et m2 petits, pouvant être à racine unique ; une m3 petite ou absente ; et un palais large. »
— Richard H. Tedford[29]
Le cladogramme ci-dessous est basé sur la phylogénie ADN de Lindblad-Toh et al. (2005)[30], modifiée pour incorporer les découvertes récentes sur les espèces de Canis[31],[32] :
| Canis |
| |||||||||||||||||||||||||||||||||||||||||||||
En 2019, un atelier organisé par le groupe de spécialistes des canidés de l'UICN/SSC recommande que, les preuves génétiques montrant que le Chacal à flancs rayés (Canis adustus) et le Chacal à chabraque (Canis mesomelas) forment une lignée monophylétique située en dehors du clade Canis/Cuon/Lycaon, ils soient placés dans un genre distinct, Lupulella Hilzheimer, 1906, sous les noms de Lupulella adusta et Lupulella mesomelas[33].
Évolution
[modifier | modifier le code]Le registre fossile montre que les féliformes et les caniformes ont émergé au sein du clade Carnivoramorpha il y a 43 millions d'années[34]. Les caniformes comprenaient le genre Leptocyon, semblable à un renard, dont diverses espèces sont apparues à partir de 24 millions d'années avant de bifurquer il y a 11,9 millions d'années en Vulpes (renards) et Canini (canins). Le genre Eucyon, de la taille d'un chacal, existait en Amérique du Nord il y a 10 millions d'années et, au début du Pliocène, environ 6 à 5 millions d'années, l'espèce Eucyon davisi[35], semblable à un coyote, a envahi l'Eurasie. Les canidés ayant émigré d'Amérique du Nord vers l'Eurasie : Eucyon, Vulpes et Nyctereutes, étaient des prédateurs de taille petite à moyenne durant le Miocène supérieur et le Pliocène inférieur, mais ils n'étaient pas les prédateurs dominants.

Pour les populations de Canis du Nouveau Monde, l'Eucyon d'Amérique du Nord a donné naissance aux premiers membres nord-américains du genre Canis, apparus pour la première fois au Miocène, il y a 6 millions d'années dans le sud-ouest des États-Unis et au Mexique. Il y a 5 millions d'années, l'espèce plus grande Canis lepophagus, ancêtre des loups, est apparue dans la même région[36].
Il y a environ 5 millions d'années, certains Eucyon de l'Ancien Monde ont évolué pour devenir les premiers membres du genre Canis[37], et la position des canidés a évolué pour devenir celle d'un prédateur dominant à travers la région paléarctique. L'espèce C. chihliensis, de la taille d'un loup, est apparue dans le nord de la Chine au milieu du Pliocène, il y a environ 4 à 3 millions d'années. Cela a été suivi par une explosion évolutive du genre Canis à travers l'Eurasie au début du Pléistocène, il y a environ 1,8 million d'années. Cet événement est associé à la formation de la steppe des mammouths et à la glaciation continentale. Le genre Canis s'est propagé en Europe sous les formes de Canis arnensis, Canis etruscus et Canis falconeri[36].
Cependant, une étude génétique de 2021 sur le Loup sinistre (Aenocyon dirus), précédemment considéré comme un membre de Canis, a révélé qu'il représentait le dernier membre d'une ancienne lignée de canins originaires du Nouveau Monde s'étant séparée avant l'apparition de Canis. Sa lignée était distincte depuis le Miocène sans preuve d'introgression avec le genre Canis. L'étude émet l'hypothèse que les canidés du Néogène du Nouveau Monde, Canis armbrusteri et Canis edwardii, étaient peut-être membres de cette lignée distincte ayant acquis par convergence évolutive une apparence très similaire aux membres du genre Canis. Les véritables membres du genre, à savoir le Loup gris et le coyote, ne seraient arrivés dans le Nouveau Monde qu'au cours du Pléistocène supérieur, où leur flexibilité alimentaire ou leur capacité à s'hybrider leur a permis de survivre à l'extinction du Quaternaire, contrairement au loup sinistre[37].
Xenocyon est un sous-genre éteint du genre Canis[38]. La diversité du groupe a diminué entre la fin du Pléistocène inférieur et le Pléistocène moyen, se limitant en Eurasie aux petits loups du groupe Canis mosbachensis–Canis variabilis et au grand hypercarnivore Canis (Xenocyon) lycaonoides[39]. L'hypercarnivore Xenocyon a donné naissance au Dhole moderne et au Lycaon[36] .
Migration africaine
[modifier | modifier le code]La première trace des espèces du genre Canis sur le continent africain est l'espèce temporairement nommée Canis sp. A de South Turkwel, au Kenya, datée de 3,58 à 3,2 millions d'années[40]. En 2015, une étude des séquences du génome mitochondrial et des séquences nucléaires du génome complet des canidés africains et eurasiatiques a indiqué que les canidés lupoïdes actuels ont colonisé l'Afrique à partir de l'Eurasie au moins à cinq reprises tout au long du Pliocène et du Pléistocène.
Ces données sont cohérentes avec les preuves fossiles suggérant qu'une grande partie de la diversité de la faune de canidés africains résulte de l'immigration d'ancêtres eurasiatiques, probablement en coïncidence avec les oscillations climatiques plio-pléistocènes entre conditions arides et humides[31]:S1. En 2017, les restes fossiles d'une nouvelle espèce du genre Canis, nommée Canis othmanii, ont été découverts parmi des vestiges trouvés à Wadi Sarrat, en Tunisie, dans des dépôts datant de 700 000 ans. Ce canidé présente une morphologie plus étroitement associée aux canidés d'Eurasie qu'à ceux d'Afrique[41].
Liste des espèces
[modifier | modifier le code]Listes passées
[modifier | modifier le code]Selon Mammal Species of the World dans sa première édition en 1982[42] :
Selon Mammal Species of the World (version 3, 2005) (11 juillet 2014)[43] :
- Canis adustus
- sous-espèce Canis adustus adustus
- sous-espèce Canis adustus bweha
- sous-espèce Canis adustus grayi
- sous-espèce Canis adustus kaffensis
- sous-espèce Canis adustus lateralis
- sous-espèce Canis adustus notatus
- Canis aureus
- sous-espèce Canis aureus algirensis
- sous-espèce Canis aureus anthus
- sous-espèce Canis aureus aureus
- sous-espèce Canis aureus bea
- sous-espèce Canis aureus cruesemanni
- sous-espèce Canis aureus ecsedensis
- sous-espèce Canis aureus indicus
- sous-espèce Canis aureus lupaster
- sous-espèce Canis aureus moreotica
- sous-espèce Canis aureus naria
- sous-espèce Canis aureus riparius
- sous-espèce Canis aureus soudanicus
- sous-espèce Canis aureus syriacus
- Canis latrans
- sous-espèce Canis latrans cagottis
- sous-espèce Canis latrans clepticus
- sous-espèce Canis latrans dickeyi
- sous-espèce Canis latrans frustror
- sous-espèce Canis latrans goldmani
- sous-espèce Canis latrans hondurensis
- sous-espèce Canis latrans impavidus
- sous-espèce Canis latrans incolatus
- sous-espèce Canis latrans jamesi
- sous-espèce Canis latrans latrans
- sous-espèce Canis latrans lestes
- sous-espèce Canis latrans mearnsi
- sous-espèce Canis latrans microdon
- sous-espèce Canis latrans ochropus
- sous-espèce Canis latrans peninsulae
- sous-espèce Canis latrans texensis
- sous-espèce Canis latrans thamnos
- sous-espèce Canis latrans umpquensis
- sous-espèce Canis latrans vigilis
- Canis lupus
- sous-espèce Canis lupus albus
- sous-espèce Canis lupus alces
- sous-espèce Canis lupus arabs
- sous-espèce Canis lupus arctos
- sous-espèce Canis lupus baileyi
- sous-espèce Canis lupus beothucus
- sous-espèce Canis lupus bernardi
- sous-espèce Canis lupus campestris
- sous-espèce Canis lupus chanco
- sous-espèce Canis lupus columbianus
- sous-espèce Canis lupus crassodon
- sous-espèce Canis lupus dingo
- sous-espèce Canis lupus familiaris
- sous-espèce Canis lupus floridanus
- sous-espèce Canis lupus fuscus
- sous-espèce Canis lupus gregoryi
- sous-espèce Canis lupus griseoalbus
- sous-espèce Canis lupus hattai
- sous-espèce Canis lupus hodophilax
- sous-espèce Canis lupus hudsonicus
- sous-espèce Canis lupus irremotus
- sous-espèce Canis lupus labradorius
- sous-espèce Canis lupus ligoni
- sous-espèce Canis lupus lupus
- sous-espèce Canis lupus lycaon
- sous-espèce Canis lupus mackenzii
- sous-espèce Canis lupus manningi
- sous-espèce Canis lupus mogollonensis
- sous-espèce Canis lupus monstrabilis
- sous-espèce Canis lupus nubilus
- sous-espèce Canis lupus occidentalis
- sous-espèce Canis lupus orion
- sous-espèce Canis lupus pallipes
- sous-espèce Canis lupus pambasileus
- sous-espèce Canis lupus rufus
- sous-espèce Canis lupus tundrarum
- sous-espèce Canis lupus youngi
- Canis mesomelas
- sous-espèce Canis mesomelas mesomelas
- sous-espèce Canis mesomelas schmidti
- Canis simensis
- sous-espèce Canis simensis citernii
- sous-espèce Canis simensis simensis
Liste des espèces actuelles
[modifier | modifier le code]| Espèce (nom binominal, nom vernaculaire et auteur) | Répartition géographique | Statut UICN mondial | Tendance de la population | Image |
|---|---|---|---|---|
| Canis familiaris
(Chien) |
Domestiqué, mondial | — | 
| |
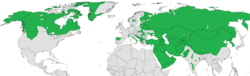
| Canis lupus
(Loup gris) |
 |

| ||
| Canis aureus
(Chacal doré) |
 |

| ||
| Canis lupaster
(Loup doré africain) |
 |

| ||
| Canis simensis
(Loup d’Abyssinie ou cabéru) |
 |

| ||
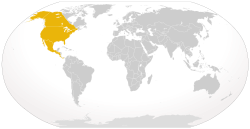
| Canis latrans
(Coyote) |
 |

| ||
| Canis rufus
(Loup rouge) |
Sud-est des États-Unis | 
| ||
| Canis lycaon
(Loup de l’Est) |
Sud du Québec et Ontario | Inconnue | 
|
Auquel on peut ajouter quatre espèces au statut discuté :
| Espèce (nom binominal, nom vernaculaire et auteur) | Répartition géographique | Statut UICN mondial | Tendance de la population | Image |
|---|---|---|---|---|
| Canis himalayensis
(Loup d'Himalaya) |
NE | Inconnue | 
| |
| Canis indica
(Loup des Indes) |
NE | Inconnue | 
|
Et peut-être 52 espèces fossiles :
Liste des espèces et sous-espèces
[modifier | modifier le code]Selon Paleobiology Database (7 novembre 2023)[62] :
- Canis (Epicyon)
- Canis accitanus
- Canis adoxus
- Canis apolloniensis
- Canis armbrusteri
- Canis arnensis
- Canis aureus
- Canis borjgali
- Canis cana
- Canis cedazoensis
- Canis ceylonicus
- Canis chihliensis
- Canis cipio
- Canis culpaeus
- Canis dingo
- Canis edwardii
- Canis etruscus
- Canis familiaris
- Canis feneus
- Canis geismarianus
- Canis gezi
- Canis hewitti
- Canis incertus
- Canis latidentatus
- Canis latrans
- Canis lepophagus
- Canis longdanensis
- Canis lupaster
- Canis lupus
- Canis lydekkeri
- Canis megamastoides
- Canis michauxi
- Canis monticinensis
- Canis mosbachensis
- Canis osorum
- Canis othmanii
- Canis palaeoplatensis
- Canis palmidens
- Canis proplatensis
- Canis rufus
- Canis sechurae
- Canis senezensis
- Canis simensis
- Canis tarijensis
- Canis teilhardi
- Canis thooides
- Canis troglodytes
- Canis variabilis
- Canis vetulus
- Nyctereutes terblanchei
Description
[modifier | modifier le code]Description et dimorphisme sexuel
[modifier | modifier le code]Il existe peu de différences morphologiques entre les mâles et les femelles chez les canidés. Ils ont tendance à vivre en couples monogames. Les loups, les coyotes et les chacals vivent en groupes comprenant des couples reproducteurs et leur progéniture. Les loups peuvent également vivre au sein de familles élargies. Pour capturer des proies plus grandes qu'eux, les loups gris dépendent de leurs mâchoires, car ils ne peuvent pas utiliser leurs membres antérieurs pour saisir leurs proies. Ils chassent en meutes composées d'un couple alpha et de leurs petits de l'année en cours et des années précédentes[63]. Les prédateurs mammifères sociaux s'attaquent généralement à des herbivores dont la masse corporelle est similaire à la masse combinée de la meute de prédateurs[64],[65]. Le loup gris se spécialise dans la capture d'individus vulnérables parmi les grandes proies[66], et une meute de loups peut abattre un élan de 500 kg[67],[68].
Dentition et force de morsure
[modifier | modifier le code]
| Canidé | Carnassière | Canine |
|---|---|---|
| Loup | 131,6 | 127,3 |
| Chien (ici Chien du Groenland et dingo) |
117,4 | 114,3 |
| Coyote | 107,2 | 98,9 |
| Chacal doré | 89,6 | 87,7 |
La dentition concerne la disposition des dents dans la gueule. La notation dentaire pour les dents de la mâchoire supérieure utilise les lettres majuscules : I pour les incisives, C pour les canines, P pour les prémolaires et M pour les molaires ; les lettres minuscules i, c, p et m désignent les dents de la mandibule. Les dents sont numérotées sur un côté de la gueule, de l'avant vers l'arrière. Chez les carnivores, la quatrième prémolaire supérieure P4 et la première molaire inférieure m1 forment les carnassières, qui agissent ensemble comme des ciseaux pour trancher les muscles et les tendons des proies[36].
Les canidés utilisent leurs prémolaires pour couper et broyer, à l'exception de la quatrième prémolaire supérieure P4 (la carnassière supérieure) qui ne sert qu'à couper. Ils utilisent leurs molaires pour broyer, sauf la première molaire inférieure m1 (la carnassière inférieure) qui a évolué pour à la fois couper et broyer, selon l'adaptation alimentaire du canidé. Sur la carnassière inférieure, le trigonide sert à trancher et le talonide à broyer. Le rapport entre le trigonide et le talonide indique les habitudes alimentaires d'un carnivore : un trigonide plus grand indique un hypercarnivore, tandis qu'un talonide plus grand indique un régime plus omnivore[70],[71]. En raison de sa faible variabilité, la longueur de la carnassière inférieure est utilisée pour fournir une estimation de la taille corporelle d'un carnivore[70].
Une étude portant sur l'estimation de la force de morsure au niveau des canines sur un large échantillon de prédateurs mammifères actuels et fossiles, ajustée selon leur masse corporelle, a révélé que pour les mammifères placentaires, la force de morsure aux canines (en newtons par kilogramme de poids corporel) était la plus élevée chez le Loup sinistre éteint (163). Parmi les canidés modernes, elle est suivie par quatre hypercarnivores qui s'attaquent souvent à des animaux plus grands qu'eux : le Lycaon (142), le Loup gris (136), le Dhole (112) et le Dingo (108). La force de morsure au niveau des carnassières montre une tendance similaire à celle des canines. La taille maximale des proies d'un prédateur est fortement influencée par ses limites biomécaniques[72].
Fracture dentaire
[modifier | modifier le code]
La fracture dentaire est une conséquence fréquente du comportement alimentaire des carnivores[73]. Les chasseurs solitaires dépendent d'une morsure puissante au niveau des canines pour maîtriser leur proie et possèdent donc une symphyse mandibulaire robuste. À l'inverse, les chasseurs en meute, qui infligent de nombreuses morsures moins profondes, ont une symphyse comparativement plus faible. Les mandibules des canidés sont renforcées derrière les carnassières pour briser les os avec leurs molaires post-carnassières (M2 et M3). Le loup gris moderne et le loup rouge (C. rufus) possèdent des renforts plus importants que tous les autres canidés actuels ou que le loup sinistre éteint, ce qui indique une meilleure adaptation au broyage des os[74].
Une étude sur neuf carnivores modernes montre qu'un adulte sur quatre a subi une fracture dentaire, dont la moitié concerne les canines. La fréquence la plus élevée se trouve chez la hyène tachetée, connue pour consommer l'intégralité de ses proies, os compris, tandis que la plus faible se trouve chez le Lycaon. Le loup gris se situe entre les deux[75]. La consommation d'os augmente le risque de fracture accidentelle en raison des contraintes imprévisibles qu'elle génère. Les canines sont les plus touchées en raison de leur forme et de leur fonction, qui les soumettent à des contraintes de flexion importantes[73],[76].
Par rapport aux loups gris actuels, les loups de Béringie présentaient des dents nettement plus usées et un nombre de fractures beaucoup plus élevé (jusqu'à 11 % contre 2 % chez le loup des Rocheuses septentrionales). Cette usure des incisives et des carnassières reflète une consommation habituelle d'os, ces derniers étant rongés avec les incisives puis brisés avec les carnassières et les molaires[77].
Comportement
[modifier | modifier le code]Reproduction
[modifier | modifier le code]Le genre Canis comprend de nombreuses espèces présentant une large gamme de comportements de reproduction variant selon la physionomie et l'espèce[78]. Une étude de 2017 a montré que chez certaines espèces, les femelles utilisent leur statut sexuel pour accéder aux ressources alimentaires. Les loups sont généralement monogames et forment des liens de couple durables, tandis que les chiens domestiques en liberté sont polygames et s'accouplent avec plusieurs individus. L'étude a révélé que, dans les deux espèces, les femelles cherchaient davantage à accéder à la nourriture et réussissaient mieux à monopoliser une ressource lorsqu'elles étaient en œstrus. En dehors de la saison de reproduction, ces efforts étaient moins persistants et moins fructueux. Cela suggère que l'hypothèse de la « nourriture contre sexe » joue un rôle dans le partage des ressources et offre un bénéfice direct aux femelles[78].
Une autre étude sur les chiens errants a montré que les facteurs sociaux influencent de manière significative le choix des partenaires. Les femelles en chaleur recherchent les mâles dominants et sont plus susceptibles de s'accoupler avec un mâle dominant perçu comme un leader de qualité, tout en rejetant les mâles soumis. De plus, la compétition entre mâles est plus agressive en présence de femelles de rang élevé. Cela suggère que les indices sociaux et le statut jouent un rôle majeur dans la formation des couples chez les chiens[79].
Les canidés font preuve d'une grande variété en ce qui concerna la mise en place des soins parentaux. Une étude de 2018 sur les coyotes a montré que l'investissement paternel augmentait pour égaler ou presque l'investissement maternel, fluctuant en fonction du niveau de soins prodigués par la mère[80]. Chez les chiens errants, les mères modifient leur investissement en temps et en énergie à mesure que les chiots grandissent : elles passent d'un soin à haute énergie à un soin à plus faible énergie pour prolonger la durée de l'accompagnement tout en réduisant leurs besoins énergétiques, augmentant ainsi les chances de survie des petits[81].
Notes et références
[modifier | modifier le code]Notes
[modifier | modifier le code]Références
[modifier | modifier le code]- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Canis » (voir la liste des auteurs).
- C. S. Rafinesque, Analyse de la Nature ou tableau de l'univers et des corps organisés, Palerme, (lire en ligne), p. 59.
- (de) L. Oken, Lehrbuch der Naturgeschichte, vol. 2, t. 3, (lire en ligne), p. 1039.
- ↑ (en) S.D.W., « The mammals of Britain systematically arranged », The Analyst, vol. 4, , p. 69 (lire en ligne).
- H. M. D. de Blainville, « Rapport sur un mémoire de M. Jourdan concernant deux nouvelles espèces de mammifères de l'Inde », Annales des Sciences Naturelles, Zoologie, seconde Série, vol. 8, , p. 279 (lire en ligne).
- (en) Ch. H. Smith, The natural history of dogs. Canidæ or genus Canis of authors, vol. 18, Édimbourg, W.H. Lizars, (lire en ligne), p. 17-266.
- (en) B. H. Hodgson, « Classified Catalogue of Mammals of Nepal », Calcutta Journal of Natural History, vol. 2, no 6, , p. 213 (lire en ligne).
- ↑ P. Gervais, Histoire naturelle des mammifères, Paris, L. Curmer, (lire en ligne), p. 60.
- (en) J. E. Gray, « Notes on the Skulls of the Species of Dogs, Wolves, and Foxes (Canidae) in the Collection of the British Museum », Proceedings of the Zoological Society of London, vol. 1868, , p. 492–525 (lire en ligne).
- (en) J. E. Gray, Catalogue of carnivorous, pachydermatous and edentate Mammalia in the British Museum, Londres, (lire en ligne), p. 180.
- ↑ J. R. Bourguignat, « Recherches sur les ossements de Canidæ constatés en France à l'état fossile pendant la période quaternaire », Annales des sciences géologiques, vol. 6, no 6, , p. 23 (lire en ligne).
- (en) E. D. Cope, « On the genera of Felidæ and Canidæ », Proceedings of the Academy of Natural Sciences of Philadelphia, vol. 31, no 2, , p. 168–194 (lire en ligne).
- ↑ (es) F. Ameghino, La antigüedad del hombre en el Plata, t. 2, Paris, , p. 306.
- ↑ (en) J. A. Allen, « On an extinct type of dog from Ely Cave, Lee County, Virginia », Memoirs of the Museum of Comparative Zoölogy, vol. 10, no 2, , p. 4 (lire en ligne).
- ↑ (es) A. L. Herrera, Sinonimia vulgar y cientifica de los principales vertebrados mexicanos, Mexico, , p. 29.
- ↑ (de) M. Hilzheimer, « Die geographische Verbreitung der afrikanischen Grau-Schakale », Der Zoologische Garten, vol. 47, , p. 365 (lire en ligne).
- ↑ (en) E. Heller, « New subspecies of mammals from equatorial Africa », Smithsonian miscellaneous collections, vol. 63, no 7, , p. 1 (lire en ligne).
- ↑ (de) I. Krumbiegel, « Der Andenwolf: Ein neuentdecktes Grosstier », Naturwissenschaftliche Wochenschrift, vol. 49, , p. 591.
- (es) O. P. Arredondo de la Mata et L. S. Varona, « Nuevos género y especie de mamífero (Carnivora: Canidae) del cuaternario de Cuba », Poeyana, vol. 131, , p. 1–12.
- ↑ (es) O. P. Arredondo de la Mata, « Reemplazo de Paracyon por Indocyon (Carnivora: Canidae) », Miscellanea Zoologica, Academie de Ciéncias de Cuba, vol. 12, , p. 4.
- ↑ (en) V. G. Heptner et N. P. Naumov, Mammals of the Soviet Union : Vol.II Part 1a, SIRENIA AND CARNIVORA (Sea Cows, Wolves and Bears), États-Unis, Science Publishers, Inc., , 124–129 p. (ISBN 1-886106-81-9).
- ↑ (en) Mammal Species of the World (3e éd., 2005) : Canis lupus Linnaeus, 1758
- ↑ Le loup à l'origine du chien ? publié en 30/08/2001 sur le site de l'UMES
- ↑ (en) Suvi Viranta, Anagaw Atickem, Lars Werdelin et Nils Chr. Stenseth, « Rediscovering a forgotten canid species », BMC Zoology, vol. 2, no 1, , p. 6 (ISSN 2056-3132, DOI 10.1186/s40850-017-0015-0, lire en ligne, consulté le )
- ↑ (en) Jan Zrzavý, Pavel Duda, Jan Robovský et Isabela Okřinová, « Phylogeny of the Caninae (Carnivora): Combining morphology, behaviour, genes and fossils », Zoologica Scripta, vol. 47, no 4, , p. 373–389 (DOI 10.1111/zsc.12293, lire en ligne, consulté le )
- ↑ (la) Carl Linnæus, Systema naturæ per regna tria naturæ, secundum classes, ordines, genera, species, Stockholm, Laurentius Salvius, (lire en ligne), p. 38
- ↑ (en) R. Wayne, « Origin, genetic diversity, and genome structure of the domestic dog », BioEssays, vol. 21, no 3, , p. 247–57 (DOI 10.1002/(SICI)1521-1878(199903)21:3<247::AID-BIES9>3.0.CO;2-Z)
- ↑ (en) « Opinion 91. Eleven Common Generic Names of Mammals Placed in the Official List of Generic Names », Smithsonian Miscellaneous Collections, vol. 73, no 4, (lire en ligne)
- ↑ (en) Opinions and Declarations Rendered by the International Commission on Zoological Nomenclature, vol. 1C, Order of the International Trust for Zoological Nomenclature, , « Direction 22 », p. 183
- ↑ (en) Richard H. Tedford et Xiaoming Wang, « Phylogenetic Systematics of the North American Fossil Caninae (Carnivora: Canidae) », Bulletin of the American Museum of Natural History, vol. 325, , p. 1–218 (lire en ligne)
- ↑ (en) Kerstin Lindblad-Toh et Claire M. Wade, « Genome sequence, comparative analysis and haplotype structure of the domestic dog », Nature, vol. 438, no 7069, , p. 803–819 (PMID 16341006, DOI 10.1038/nature04338)
- (en) Klaus-Peter Koepfli et John Pollinger, « Genome-wide evidence reveals that African and Eurasian Golden Jackals are distinct species », Current Biology, vol. 25, no 16, , p. 2158–2165 (PMID 26234211, DOI 10.1016/j.cub.2015.06.060)
- ↑ (en) Paul J. Wilson et Sonya Grewal, « DNA profiles of the eastern Canadian wolf and the red wolf provide evidence for a common evolutionary history independent of the gray wolf », Canadian Journal of Zoology, vol. 78, no 12, , p. 2156–2166 (DOI 10.1139/z00-158).
- ↑ (en) Francisco Alvares, Wieslaw Bogdanowicz et Liz A.D. Campbell, « Old World Canis spp. with taxonomic ambiguity: Workshop conclusions and recommendations », sur IUCN/SSC Canid Specialist Group, (consulté le )
- ↑ (en) John J. Flynn et Gina D. Wesley-Hunt, « Phylogeny of the Carnivora: Basal Relationships Among the Carnivoramorphans », Journal of Systematic Palaeontology, vol. 3, , p. 1–28 (DOI 10.1017/s1477201904001518)
- ↑ (en) « Eucyon davisi », sur Fossilworks (consulté le )
- (en) Xiaoming Wang et Richard H. Tedford, Dogs: Their Fossil Relatives and Evolutionary History, New York, Columbia University Press, (ISBN 978-0-231-13529-0), p. 1–232
- (en) Angela R. Perri, Kieren J. Mitchell et Alice Mouton, « Dire wolves were the last of an ancient New World canid lineage », Nature, vol. 591, no 7848, , p. 87–91 (DOI 10.1038/s41586-020-03082-x).
- ↑ (it) L. Rook, « The Plio-Pleistocene Old World Canis (Xenocyon) ex gr. falconeri », Bolletino della Società Paleontologica Italiana, vol. 33, , p. 71–82
- ↑ (en) M Sotnikova, « Dispersal of the Canini (Mammalia, Canidae: Caninae) across Eurasia during the Late Miocene to Early Pleistocene », Quaternary International, vol. 212, no 2, , p. 86–97 (DOI 10.1016/j.quaint.2009.06.008)
- ↑ (en) Lars Werdelin et Margaret E. Lewis, « Plio-Pleistocene Carnivora of eastern Africa: Species richness and turnover patterns », Zoological Journal of the Linnean Society, vol. 144, no 2, , p. 121 (DOI 10.1111/j.1096-3642.2005.00165.x).
- ↑ (en) Lamjed Amri, Saverio Bartolini Lucenti, Moncef Saïd Mtimet, Narjess Karoui-Yaakoub, Sergio Ros-Montoya, Maria-Patrocinio Espigares, Mabrouk Boughdiri, Nebiha Bel Haj Ali et Bienvenido Martínez-Navarro, « Canis othmanii sp. nov. (Carnivora, Canidae) from the early Middle Pleistocene site of Wadi Sarrat (Tunisia) », Comptes Rendus Palevol, vol. 16, no 7, , p. 774 (DOI 10.1016/j.crpv.2017.05.004).
- ↑ (en) Mammal Species of the World: A Taxonomic and Geographic Reference, Lawrence, Allen Press et Association of Systematics Collections, , 694 p. (ISBN 0-935868-01-1), p. 244
- ↑ Mammal Species of the World (version 3, 2005), consulté le 11 juillet 2014.
- ↑ José R. Castelló (trad. Anne Saint Girons), Les canidés du Monde : Loups, chiens sauvages, renards, chacals, coyotes, et apparentés, Paris, Delachaux et Niestlé, coll. « Guide Delachaux », , 332 p. (ISBN 978-2-603-02695-3, lire en ligne), p. 8
- ↑ ASM Mammal Diversity Database, consulté le 5 août 2025.
- ↑ Référence Organismnames.com : Canis antiquus Laurillard 1843 consulté le=26 février 2022.
- ↑ (en) P. N. Bose, « Undescribed Fossil Carnivora from the Siválik Hills in the Collection of the British Museum », Quarterly Journal of the Geological Society of London, Londres, Société géologique de Londres, vol. 36, nos 1-4, , p. 119-136 (ISSN 0370-291X et 2058-105X, OCLC 1437164, DOI 10.1144/GSL.JGS.1880.036.01-04.13, lire en ligne)., p. 135.
- ↑ (en) Oswaldo Mooser et Walter W. Dalquest, « Pleistocene mammals from Aguascalientes, central Mexico », Journal of Mammalogy, vol. 56, no 4, , p. 781-820 (lire en ligne).
- ↑ (es) M. Crusafont-Pairó, « El primer representante del género Canis en el pontiense euroasiático (Canis cipio) », Boletín de la Real Sociedad Española de Historia Natural, Madrid, vol. 48, , p. 43-56 (ISSN 0583-7499).
- ↑ Charles Depéret, Les animaux pliocènes du Roussillon, Paris, Librairie Polytechnique Baudry, , 194 p..
- ↑ (en) Charles Lewis Gazin, « The late cenozoic vertebrate faunas from the San Pedro Valley, Ariz. », Proceedings of the United States National Museum, vol. 92, no 3155, , p. 475-518 (lire en ligne).
- ↑ (en) Wade E. Miller et Oscar Carranza-Castañeda, « Late Tertiary Canids from Central Mexico », Journal of Paleontology, vol. 72, no 3, , p. 546-556 (lire en ligne).
- ↑ Référence Organismnames.com : Thos khomenkoi Bogachev 1938 consulté le=26 février 2022.
- ↑ (en) C. Stuart Johnston, « Preliminary report on the vertebrate type locality of Cita Canyon, and the description of an ancestral coyote », Am J Sci, vol. 35, no 5, , p. 383-390 (DOI 10.2475/ajs.s5-35.209.383, lire en ligne).
- ↑ Référence Organismnames.com : Canis medius Blainville, 1843 consulté le=26 février 2022.
- ↑ (en) Richard Lydekker, « Contributions to a knowledge of the fossil vertebrates of Argentina. Part II. 3. On two argentine extinct carnivores. », Anales del Museo de La Plata. Paleontología Argentina, vol. 3, no 3, , p. 1-3.
- ↑ E. Ray Lankester, « On new Mammalia from the Red Crag », Annals and Magazine of Natural History: Series 3, vol. 14, no 83, , p. 353-360 (lire en ligne).
- ↑ Référence Organismnames.com : Canis robustus (Ameghino, 1889) consulté le=26 février 2022.
- ↑ (de) Johann Woldřich, « Über Caniden aus dem Diluvium », Denkschriften der Kaiserlichen Akademie der Wissenschaften. Mathematisch-naturwissenschaftliche Klasse, Vienne, Inconnu, vol. 39, no 2, , p. 97-148 (ISSN 0379-0207, OCLC 1478736, lire en ligne)., p. 116.
- ↑ Référence Organismnames.com : Cynodon velaunus (Aymard, 1846) consulté le=27 février 2022.
- ↑ (zh) Yuzhu You & Guoqin Qi, 1972 : « New Material from the Pleistocene Mammal Fauna at Yuanmou, Yunnan ». Vert. PalAs, vol. 11, n. 1, p. 66-85.
- ↑ Paleobiology Database, consulté le 7 novembre 2023.
- ↑ (en) Blaire Van Valkenburgh et Tyson Sacco, « Sexual dimorphism, social behavior, and intrasexual competition in large Pleistocene carnivorans », Journal of Vertebrate Paleontology, vol. 22, , p. 164–169 (DOI 10.1671/0272-4634(2002)022[0164:SDSBAI]2.0.CO;2)
- ↑ (en) Boris Sorkin, « A biomechanical constraint on body mass in terrestrial mammalian predators », Lethaia, vol. 41, no 4, , p. 333–347 (DOI 10.1111/j.1502-3931.2007.00091.x)
- ↑ (en) M. Earle, « A flexible body mass in social carnivores », American Naturalist, vol. 129, no 5, , p. 755–760 (DOI 10.1086/284670)
- ↑ (en) P Paquet et L. W. Carbyn, Wild Mammal of North America: Biology, Management, and Conservation, Nature, , 482–509 p. (ISBN 978-0-8018-7416-1), « 23-Gray Wolf (Canis Inpus and Allies) »
- ↑ (en) L. David Mech, The Wolves of Isle Royale, Fauna of the National Parks of the United States, (ISBN 978-1-4102-0249-9), p. 76
- ↑ (en) William Anyonge et Chris Roman, « New body mass estimates for Canis dirus, the extinct Pleistocene dire wolf », Journal of Vertebrate Paleontology, vol. 26, , p. 209–212 (DOI 10.1671/0272-4634(2006)26[209:NBMEFC]2.0.CO;2)
- ↑ (en) Per Christiansen et Stephen Wroe, « Bite Forces and Evolutionary Adaptations to Feeding Ecology in Carnivores », Ecology, vol. 88, no 2, , p. 347–358 (PMID 17479753, DOI 10.1890/0012-9658(2007)88[347:bfaeat]2.0.co;2)
- (en) Gabriele Sansalone et Davide Federico Bertè, « Evolutionary trends and stasis in carnassial teeth of European Pleistocene wolf Canis lupus », Quaternary Science Reviews, vol. 110, , p. 36–48 (DOI 10.1016/j.quascirev.2014.12.009)
- ↑ (en) Marco Cherin et Davide Federico Bertè, « Canis etruscus (Canidae, Mammalia) and its role in the faunal assemblage from Pantalla (Perugia, central Italy) », Bollettino della Società Paleontologica Italiana, vol. 52, no 1, , p. 11–18 (lire en ligne)
- ↑ (en) S. Wroe et C. McHenry, « Bite club: Comparative bite force in big biting mammals », Proceedings of the Royal Society B, vol. 272, no 1563, , p. 619–25 (DOI 10.1098/rspb.2004.2986)
- (en) B Van Valkenburgh, « Incidence of tooth breakage among large predatory mammals », Am. Nat., vol. 131, no 2, , p. 291–302 (DOI 10.1086/284790)
- ↑ (en) François Therrien, « Mandibular force profiles of extant carnivorans and implications for the feeding behaviour of extinct predators », Journal of Zoology, vol. 267, no 3, , p. 249–270 (DOI 10.1017/S0952836905007430)
- ↑ (en) Blaire Van Valkenburgh et Fritz Hertel, « Tough Times at La Brea: Tooth Breakage in Large Carnivores of the Late Pleistocene », Science, vol. 261, no 5120, , p. 456–459 (DOI 10.1126/science.261.5120.456)
- ↑ (en) L.R.G. DeSantis, « Dental microwear textures of carnivorans from the La Brea Tar Pits, California and potential extinction implications », Science Series 42, Natural History Museum of Los Angeles County, (consulté le )
- ↑ (en) Jennifer A. Leonard et Carles Vilà, « Megafaunal Extinctions and the Disappearance of a Specialized Wolf Ecomorph », Current Biology, vol. 17, no 13, , p. 1146–50 (PMID 17583509, DOI 10.1016/j.cub.2007.05.072)
- (en) Rachel Dale, Sarah Marshall-Pescini et Friederike Range, « Do females use their sexual status to gain resource access? Investigating food-for-sex in wolves and dogs », Current Zoology, vol. 63, no 3, , p. 323–330 (PMID 29491991, PMCID 5804177, DOI 10.1093/cz/zow111).
- ↑ (en) Simona Cafazzo, Roberto Bonanni, Paola Valsecchi et Eugenia Natoli, « Social Variables Affecting Mate Preferences, Copulation and Reproductive Outcome in a Pack of Free-Ranging Dogs », PLOS ONE, vol. 9, no 6, (PMID 24905360, PMCID 4048177, DOI 10.1371/journal.pone.0098594).
- ↑ (en) Christopher J. Schell, « It takes two: Evidence for reduced sexual conflict over parental care in a biparental canid », Journal of Mammalogy, vol. 99, no 1, , p. 75–88 (DOI 10.1093/jmammal/gyx150).
- ↑ (en) Manabi Paul, « Clever mothers balance time and effort in parental care: a study on free-ranging dogs », Royal Society Open Science, vol. 4, no 1, (PMID 28280555, PMCID 5319321, DOI 10.1098/rsos.160583).
Annexes
[modifier | modifier le code]Articles connexes
[modifier | modifier le code]Noms vernaculaires du genre :
Liens externes
[modifier | modifier le code]- (en) Catalogue of Life : Canis Linnaeus, 1758 (consulté le )
- (fr + en) ITIS : Canis Linnaeus, 1758 (consulté le )
- (en) Mammal Species of the World (3e éd., 2005) : Canis Linnaeus, 1758 (consulté le )
- (en) Paleobiology Database : Canis Linnaeus 1758 (consulté le )
- (en) Animal Diversity Web : Canis (consulté le )
- (fr + en) CITES : genre Canis (sur le site de l’UNEP-WCMC) (consulté le )
- (en) Fauna Europaea : Canis Linnaeus, 1758 (consulté le )
- (en) North American Mammals : Canis (consulté le )
- (en) NCBI : Canis (taxons inclus) (consulté le )
- (en) UICN : taxon Canis (consulté le )








